《细胞》又发文!破解“铁死亡”调控密码
“铁死亡”是铁离子依赖性调控性细胞死亡,其启动、进程与转归由细胞铁池稳态、谷胱甘肽抗氧化、脂质过氧化三大核心轴共同决定。过去十多年,科学家们的研究主要围绕抗氧化与脂质过氧化通路展开,发现了GPX4、FSP1等关键靶点,但真正起决定性作用的“细胞铁池”精密调控机制,一直是学术界悬而未决的问题。
北京时间4月27日,《细胞》期刊发表了题为《Stabilizing MARCH7 as a ferro-guardian against ferroptosis》的研究论文。该研究首次发现了细胞铁代谢的核心调控蛋白MARCH7,填补了“铁死亡”领域上游铁调控机制的核心空白,为今后“铁死亡”相关疾病的药物研发提供全新的思路。
该论文的第一通讯单位为浙江大学医学院。第一通讯作者为张强。浙江大学医学院教授王福俤、闵军霞,上海中医药大学附属市中医医院研究员巴乾为共同通讯作者。浙江大学医学院2021级博士生研究生黄文祥、2022级博士生研究生王睿君,博士后杨鑫泉和杨双杰为共同第一作者。

“铁死亡”的关键突破
“铁死亡”的发生,依赖于细胞内铁过载所驱动的脂质过氧化。近年来,“铁死亡”已被证实广泛参与多种重大疾病的病理进程,包括肿瘤、心力衰竭与心肌梗死等心血管疾病、肝脏疾病、肾脏损伤等疾病,成为极具潜力的治疗靶点。
此前,学术界对铁进入细胞(通过TFR1受体)以及铁从铁蛋白储存库中释放(通过NCOA4介导的铁蛋白自噬)已有基本认识——TFR1和NCOA4堪称铁代谢调控的两员干将,但一个根本性的问题始终存在:在这两员干将之上,是否还有一位更上游的“统帅”,能够统一调度铁的流入与流出?

2021年以来,团队围绕泛素-蛋白酶体系统调控“铁死亡”开展攻关,逐步建立起“泛素化多组学”研究策略——一种能够全方位扫描细胞内蛋白质“泛素化标签”的高精度技术,并结合“高通量功能验证体系”,最终确证 E3泛素连接酶MARCH7是“铁死亡”中调控铁代谢的关键分子,填补了“铁死亡”领域上游铁调控机制的关键空白。
拧紧“铁”的两个龙头
那这个叫MARCH7的蛋白,究竟是怎么工作的呢?
团队在后续的实验摸索中,逐渐明晰了MARCH7 介导铁稳态调控、进而抑制“铁死亡”的完整分子机制:
一方面,MARCH7蛋白给细胞表面的TFR1蛋白打上泛素化标签,关上铁离子进入细胞的大门,减少铁离子从外面进入细胞;
另一方面,给细胞里负责“搬铁”的NCOA4蛋白打上泛素化标签,把它降解掉,这样铁离子就被牢牢锁在细胞内的“仓库”里,不会到处乱跑。
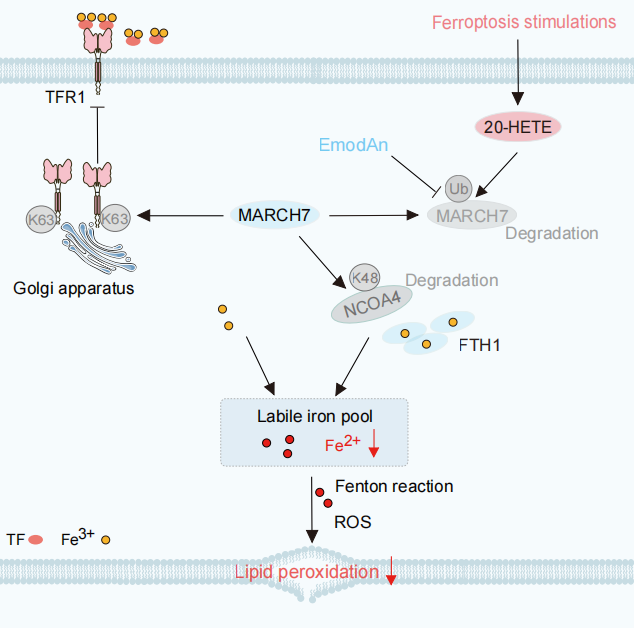
MARCH7介导铁代谢和铁死亡的机制分析
简单来说,MARCH7蛋白相当于一个“上游总开关”,通过管控“铁代谢”的“进口”和“出口”,从源头和储存两个方向同时发力,最终让细胞内的铁元素保持在稳定状态。这一发现为理解细胞如何主动限制铁过载以抵御“铁死亡”,提供了新的分子机制。
从实验室走向治疗
发现新靶点后,团队进一步开发了一种 MARCH7荧光探针——可以实时“看到”这个蛋白的活跃程度和变化。
接着,他们利用高内涵筛选系统从6000多个分子中鉴定出多个能稳定MARCH7、防止其降解的小分子。这些小分子能防止MARCH7在铁元素过载的场景下“自毁”,从而让它稳定发挥对铁元素的调控作用。
更令人振奋的是,在心肌损伤和铁过载相关心脏病这两种心脏疾病的动物模型中,这些小分子药物显著稳定了MARCH7蛋白水平,有效挽救了心肌组织损伤,抑制了心脏细胞的“铁死亡”。
这一发现证实,靶向激活内源性“铁卫士”MARCH7,是更高效、更安全的干预策略,可广泛应用于脂肪肝、心肌病、肿瘤疾病等铁稳态失衡相关重大疾病,为相关疾病的药物研发提供新的应对之策。