王福俤与闵军霞团队再次揭秘铁死亡引发心脏疾病的新靶点及新机制
近日,心血管领域国际著名学术期刊《Circulation Research》(影响因子:15.862)在线发表了浙江大学医学院王福俤/闵军霞教授团队题为“Loss of cardiac Ferritin H facilitates cardiomyopathy via Slc7a11-mediated ferroptosis”的研究论文【1】。该成果系统阐明了铁蛋白(Ferritin)通过调控铁死亡抑制心肌病发生的效应及分子调控机制;首次体内揭示膜蛋白Slc7a11能够通过阻断心肌细胞发生铁死亡而有效逆转铁蛋白缺失导致的心肌病,有望成为心脏疾病防治新靶点。
此外,该研究在国际上率先构建了多个心脏铁死亡的遗传小鼠模型(Ferritin H cKO),为靶向心肌细胞铁死亡提供了新模型。
该成果不仅阐明了心肌细胞“死”(铁死亡)的新机制,还颠覆性地发现挽救(生)心肌损伤/死亡的新策略——激活心肌细胞SLC7A11,即起‘死’回生。

图1. Circulation Research 论文online首页
死亡是鲜为人知的心脏新杀手
心脏疾病是人类健康的头号杀手,其分子机制与转化研究业已成为迫在眉睫的重大公共卫生及医学课题。心肌细胞作为一种典型的非分裂细胞,一旦发生损伤则成为永久性缺失的细胞(永久性细胞),其死亡是心脏损伤与疾病的共同致病基础。因此,探究心肌细胞死亡的调控机制具有重大的研究价值与临床转化意义。一直以来,抑制心肌细胞死亡是保护心脏功能、防治心脏疾病的关键策略。
2019年初,王福俤教授课题组在《PNAS》发表了题为“Ferroptosis as a target for protection against cardiomyopathy”的研究论文,该研究成果在全球范围内首次阐明了新型细胞死亡方式—铁死亡(Ferroptosis)在心脏疾病发生发展中的重要作用【2】。论文发表后,国际铁死亡研究权威、德国亥姆霍兹研究中心Marcus Conrad教授在《Cell Research》发表了题为“Broken hearts: Iron overload, ferroptosis and cardiomyopathy”的“研究亮点”(Research Highlight)文章,高度评价了这一重要成果【3】。此外,心血管研究领域顶级期刊《Circulation》以“New Target to Protect Against Cardiomyopathy”为题高度评价了该成果对领域的重要贡献【4】。截止目前,该论文被引用66次,被ESI评选为年度“高被引论文”(Highly Cited Paper)和“热点论文”(Hot Paper)。

图2. 王福俤团队2019年PNAS论文与评价
铁蛋白基因敲除加速心脏铁死亡
多年来,王福俤团队在心肌细胞铁死亡领域的深入探索过程中,利用Cre/LoxP技术构建了编码铁蛋白重链(Ferritin H, Fth)基因的心肌细胞特异性敲除小鼠(FthMCK/MCK和FthMyh6/Myh6)。铁蛋白由重链(Fth)和轻链(Ftl)两种亚基构成球壳空腔结构,是细胞内最主要的储铁蛋白。胞质中未被利用或排出细胞的铁离子被储存在铁蛋白中,从而维持细胞内铁稳态,减少Fenton反应导致的氧化应激,达到保护细胞的目的。心肌细胞特异性敲除Fth后,小鼠心脏铁代谢发生明显紊乱,并在6月龄时表现出轻度心脏损伤。为了进一步明确Fth在心肌细胞铁稳态中的功能,研究者们给小鼠增加了一定的铁负荷压力,即高铁饲料(High-iron diet,HID)喂养小鼠4周后,心肌细胞特异性Fth敲除小鼠出现心肌肥大并伴有严重的心肌损伤,呈现典型肥厚型心肌病表现。
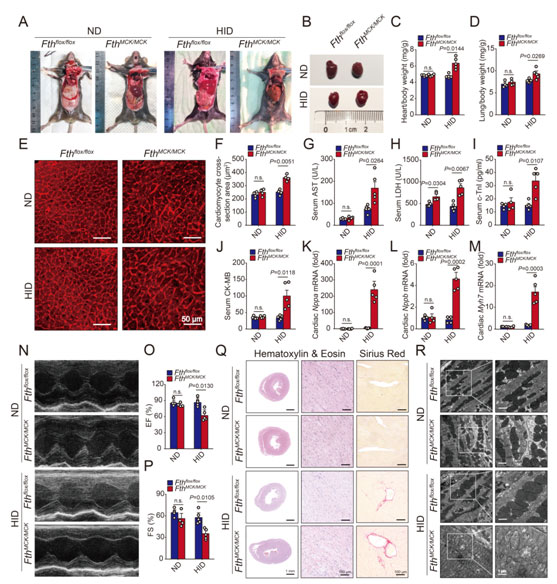
图3. Fth条件性敲除小鼠展现心肌病表型
(选自论文,Figure 3)
为了探索分子调控机制,研究人员收集心脏样本并进行转录组测序(RNA-seq)筛选;发现“铁死亡”及其密切相关的“谷胱甘肽代谢”通路在Fth敲除的心肌组织中显著上调。进一步研究提示:心肌细胞膜上胱氨酸/谷氨酸反向转运体的功能亚基Slc7a11下调而导致的胞内胱氨酸和还原型谷胱甘肽(GSH)缺乏是诱发心肌细胞发生铁死亡的主要机制。
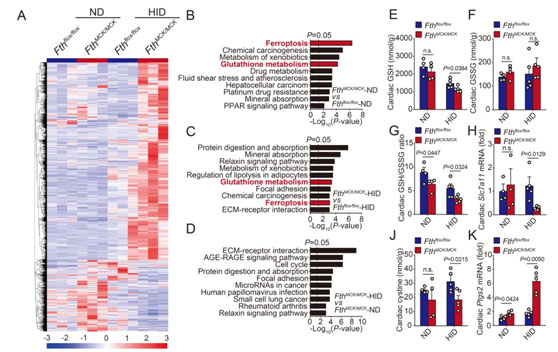
图4.转录组分析发现铁死亡和谷胱甘肽代谢通路
(选自论文,Figure 4)
铁死亡是否是HID导致心肌细胞Fth敲除小鼠的心脏结构和功能发生异常的关键机制呢?为了回答这一关键科学问题,研究者们运用铁死亡特异性抑制剂Ferrostatin-1(Fer-1)在HID饲喂的同时隔天给予小鼠腹腔注射,结果发现Fer-1处理组小鼠的心脏肥大显著减轻,心脏功能障碍也得到明显缓解,表明铁死亡的确是心脏损伤的罪魁祸首。
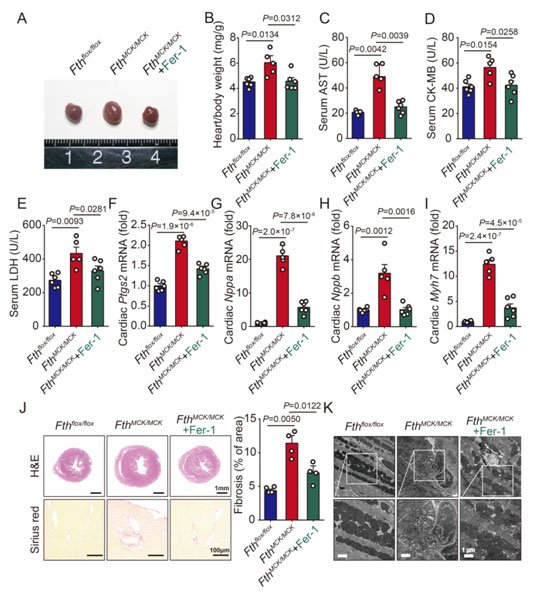
图5. 铁死亡抑制剂有效逆转心脏损伤
(选自论文,Figure 6)
过表达胱氨酸转运蛋白SLC7A11逆转心脏铁死亡
Slc7a11的下调是诱发Fth敲除小鼠心脏铁死亡的关键,那么Slc7a11过表达是否对铁死亡及其引发的心脏损伤有影响呢?研究团队在国际上首次成功制备了心肌细胞特异性Slc7a11过表达小鼠,通过与心肌细胞特异性Fth敲除小鼠进行杂交后成功获得Slc7a11过表达的Fth缺失小鼠。研究人员惊喜地发现:Slc7a11过表达通过增加细胞内的胱氨酸促进GSH合成,从而成功逆转了Fth心肌细胞敲除小鼠的铁死亡及其诱发的心衰表型。这些结果既明确了GSH缺乏是诱发Fth敲除小鼠发生心脏铁死亡这一分子机制,同时提示Slc7a11有望成为治疗铁死亡相关心脏疾病的重要靶点。
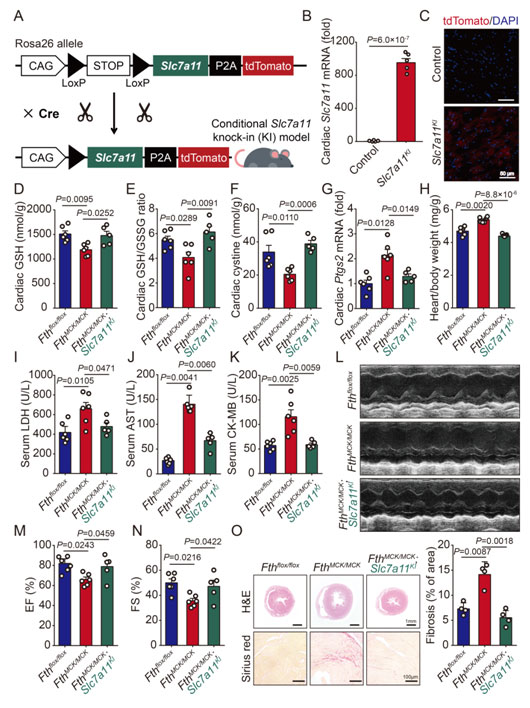
图6. 心肌细胞特异性过表达Slc7a11逆转Fth缺失导致的心脏损伤
(选自论文,Figure 7)
总之,该成果首次揭示Fth心脏特异性敲除小鼠的心力衰竭和心脏损伤的表型主要是通过心肌细胞铁死亡发生的新机制;提供了多个可靠的新型心脏铁死亡小鼠模型,不仅为阐明心脏铁死亡发生的分子调控机制提供理论依据,同时为铁死亡相关心脏疾病的防治提供了新靶点和新策略。
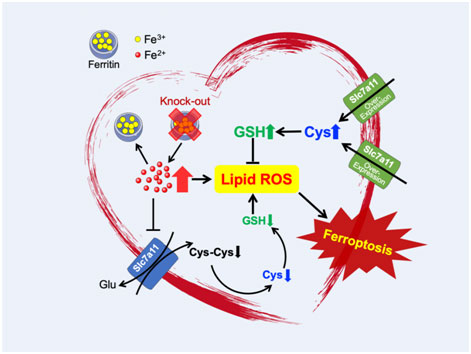
图7. 心肌细胞铁死亡模式图(选自论文)
王福俤团队博士后方学贤为论文第一作者;浙江大学王福俤教授、闵军霞教授为共同通讯作者。此项研究得到了德国德累斯顿工业大学Andreas Linkermann教授、中国医学科学院陈厚早研究员、浙江大学转化医学研究院陈静海教授的大力帮助;项目受到国家重点研发计划、国家自然科学基金以及中国博士后科学基金的经费资助。

图8. 论文通讯作者及第一作者
右起:方学贤博士(第一作者),王福俤教授(中)以及闵军霞教授
铁死亡是王福俤和闵军霞教授团队重点协同攻关的主要研究方向。通过多年来的不懈努力,团队取得系列相关研究成果。2017年在《Hepatology》杂志发表封面论文,首次报道铁死亡是铁过载导致肝脏病理损伤的重要机制并首次揭示了转运蛋白SLC7A11体内参与调控肝脏细胞铁死亡的过程【5】;之后在《PNAS》刊文首次揭示了阿霉素引发心肌病与心肌缺血再灌注损伤的两种重要体内模型中存在铁死亡及其重要意义,并阐明线粒体膜的脂质过氧化是心肌细胞发生铁死亡的关键机制【2】;团队应邀在《科学通报》发表题为“铁过载及铁死亡在心脏疾病中的研究进展”的封面评述,化用上古神话“女娲补天”形象展示靶向铁死亡防控心脏疾病的转化研究及潜在临床应用的积极前景【6】。

《Hepatology》封面(左)《科学通报》封面(右)
原文链接:www.ahajournals.org/doi/abs/10.1161/CIRCRESAHA.120.316509
参考文献
【1】Xuexian Fang , Zhaoxian Cai, Hao Wang, Dan Han, Qi Cheng, Pan Zhang, Feng Gao, Yingying Yu, Zijun Song, Qian Wu, Peng An, Sicong Huang, Jianwei Pan, Hou-Zao Chen, Jinghai Chen, Andreas Linkermann, Junxia Min, and Fudi Wang. Loss of cardiac Ferritin H facilitates cardiomyopathy via Slc7a11-mediated ferroptosis. Circulation Research, 2020, Epub ahead of print.
【2】Xuexian Fang, Hao Wang, Dan Han, Enjun Xie, Xiang Yang, Jiayu Wei, Shanshan Gu, Feng Gao, Nali Zhu, Xiangju Yin, Qi Cheng, Pan Zhang, Wei Dai, Jinghai Chen, Fuquan Yang, Huang-Tian Yang, Andreas Linkermann, Wei Gu, Junxia Min and Fudi Wang. Ferroptosis as a target for protection against cardiomyopathy. Proc Natl Acad Sci U S A. 2019;116(7):2672-2680.
【3】Marcus Conras and Bettina Proneth. Broken hearts: Iron overload, ferroptosis and cardiomyopathy. Cell Res. 2019;29(4):263-264.
【4】Tracy Hampton. New target to protect against cardiomyopathy. Circulation. 2019; 139:2278-2279.
【5】Hao Wang, Peng An, Enjun Xie, Qian Wu, Xuexian Fang, Hong Gao, Zhuzhen Zhang, Yuzhu Li, Xudong Wang, Jiaying Zhang, Guoli Li, Lei Yang, Wei Liu, Junxia Min and Fudi Wang. Characterization of ferroptosis in murine models of hemochromatosis. Hepatology, 2017, 66(2):449-65.
【6】方学贤, 蔡昭贤, 王浩, 闵军霞, 王福俤. 铁过载及铁死亡在心脏疾病中的研究进展. 科学通报. 2019, 64:2974-2987.
专家点评一
阎锡蕴:中国科学院院士,中科院生物物理研究所研究员
神奇的铁蛋白(Ferritin)是一种由24个亚基构成的储铁蛋白,它具有水合氧化铁内核及笼形蛋白质外壳,外径12~13nm,空心直径约为8nm,铁核中可积累多达4000个铁原子。Ferritin亚基由重链(Fth)和轻链(Ftl)组成,由于Fth具备催化亚铁离子(Fe2+)转化为三价铁离子(Fe3+)的亚铁氧化酶活性,因此在生物体内表现出多种重要的生理功能。临床上,铁蛋白不仅被广泛应用于疾病诊断的标志物,如缺铁性贫血、铁过载、炎症反应及肿瘤标志物等,而且作为新型纳米酶能够特异性靶向肿瘤细胞,是一种十分理想的纳米药物载体。近期,欣喜地看到多年从事铁稳态代谢的王福俤教授团队又一次带给我们有关铁蛋白的最新里程碑式研究成果。
该成果利用心肌细胞特异敲除小鼠,在体内首次揭示Fth对心脏的重要保护作用。王福俤团队研究发现:Fth敲除造成游离铁离子增多,进而通过铁死亡机制损伤心肌细胞并可发展为致死性心脏疾病。该成果清晰展示和解析了铁蛋白缺失导致心脏疾病发生发展的致病轨迹,为Fth这样一个“经典”基因完美诠释了其调控心脏铁死亡的首个体内新证据。据悉该发现是王福俤团队在铁死亡研究领域获得系列重大原创成果基础上的又一重磅硕果。
总之,该重大科技成果主要有三个方面突出贡献:(1)首次体内揭示Fth在心脏生理病理中的重要功能;(2)揭秘 Fth和Slc7a11是防治铁死亡引发心脏疾病的新靶点,具有广阔临床转化前景;(3)在国际上建立首个“心脏铁死亡”以及“铁死亡逆转”小鼠模型,为进一步药物筛选及铁死亡机制研究提供先进的研究模型。
专家点评二
杨黄恬:中国科学院上海营养与健康研研究所 研究员 研究组组长
J Mol Cell Cardiol 期刊副主编
心脏疾病是严重威胁人类生命健康的头号杀手。引发心脏疾病的致病因素众多而且机制复杂,迄今,对于心肌病及心力衰竭(心衰)等致死性疾病尚缺乏有效根治的方法,因此心脏疾病的防治一直是全球医学及生命科学领域重点攻关的热点及难点。早在2019年初,王福俤教授率领的科研团队利用小鼠模型在全球首次报道铁死亡是引发缺血/再灌等多种心脏损伤的重要致病机制(PNAS,2019)。该里程碑式成果为靶向铁死亡治疗缺血性心脏病开创了历史先河,因而获得领域同行的高度关注和点评。令人欣喜的是新近王福俤教授率领的团队在这一研究领域取得了新突破——揭秘维持心肌细胞铁稳态平衡、保护心脏对抗铁死亡引发心肌病的新靶点及新机制。研究发现为心肌病的治疗提供了新思路和新靶点。
2020年4月30日在Circ Res在线报道了王福俤教授率领的科研团队的最新研究发现(https://www.ahajournals.org/doi/abs/10.1161/CIRCRESAHA.120.316509)。作者通过采用小鼠遗传学技术成功构建了心衰特征明显的“心脏铁死亡”小鼠模型(铁蛋白重链心肌细胞特异敲除);通过全基因组转录测序技术筛查“心脏铁死亡”小鼠心肌细胞基因谱,研究人员首先发现了Slc7a11表达被显著抑制。通过巧妙的反向思维,他们构建心脏特异过表达Slc7a11小鼠模型并通过与转铁蛋白蛋白心肌细胞敲除小鼠杂交,结果发现过表达Slc7a11基因能够显著逆转“心脏铁死亡”导致的心肌损伤及预防扩张型心肌病(DCM)的发生。进一步通过氨基酸组学分析结合功能验证,作者首次揭示了Slc7a11通过增加心肌细胞内的胱氨酸促进谷胱甘肽(GSH)大量合成,结果清除脂质过氧化在心肌细胞中的堆积,从而成功逆转转铁蛋白缺失引发的铁死亡、心肌损伤及DCM的发生。DCM是引起心衰、心律失常和猝死的常见疾病之一,致死率高且缺乏有效治疗措施。该开创性发现为靶向心脏铁死亡防治心脏疾病的临床转化研究奠定了坚实的科学依据,并为破解多年来困扰国际DCM临床有效防治的难题提供了重要线索。
专家点评三
周斌:中国科学院分子细胞科学卓越创新中心研究员,国家杰青
铁死亡(Ferroptosis)是铁离子依赖的新型程序性细胞死亡方式。早在2012年,铁死亡是基于体外(In Vitro)细胞模型中观察到的一种既非凋亡又非坏死而且能被铁螯合剂挽救的细胞死亡方式(Cell,2012),之后人们逐渐认识到铁死亡可能引发肾脏及肝脏等重要脏器损伤并参与神经退行性等疾病的发生发展。因此短短几年,铁死亡已经成为全球生命科学研究热点。浙江大学医学院王福俤/闵军霞团队在2017年利用基因敲除小鼠模型探索发现铁死亡是铁过载诱发肝脏损伤中的重要致病机制(Hepatology,2017,封面论文)。由于这一成果在小鼠体内(In Vivo)首次揭示胱氨酸转运蛋白Slc7a11通过调控铁死亡参与血色病小鼠肝损伤的发病机制而备受国际学术界重视。
心肌细胞死亡是多种心脏疾病发生过程的共同病理基础,因而解读心肌死亡方式一直是生命医学领域重点关注的关键科学问题。2019年初,王福俤团队在国际上率先揭示铁死亡引发心肌细胞损伤的新机制(PNAS,2019),自此开辟了“心脏与铁死亡”研究先河。近期,国际知名学术期刊《Circulation Research》刊登了王福俤团队令人振奋的最新研究成果。通过系统性研究,作者首先锁定铁蛋白重链(Ferritin H,Fth)基因可能参与铁死亡。Fth是组成铁蛋白的两种亚基之一,通过其亚铁氧化酶活性催化亚铁离子(Fe2+)转化为三价铁离子(Fe3+),从而发挥限制二价铁和过氧化氢之间发生的有害芬顿反应(Fenton reaction)的重要生理功能。为了体内验证,作者团队利用Cre/LoxP技术制备了两种心肌细胞特异性Fth敲除小鼠模型,提供遗传学实验数据证明这些Fth缺失小鼠的心肌细胞的确发生了铁死亡。这是国际上第一个“心脏铁死亡”的遗传小鼠模型,为深入探索部分心脏疾病发生的病理机制及研发靶向铁死亡防治心脏疾病的药物提供可靠动物模型。
此外,该铁死亡领域中里程碑式研究成果还为今后研究心脏铁死亡提供了另一新型小鼠模型,即膜蛋白Slc7a11的心脏组织特异表达的转基因小鼠。研究者们充分展示过表达Slc7a11小鼠显著逆转Fth缺失诱发的心肌损伤表型;完美解读了Slc7a11通过增加细胞内的胱氨酸转运及促进GSH合成而发挥抑制铁死亡发生的关键分子调控机制;明确了Slc7a11是心脏疾病防控的重要新靶点,为心脏疾病诊治提供了崭新思路。